利用凱氏定氮儀測量牛乳中蛋白質的含量
在用國標法測定牛乳中的蛋白質時,采用多孔井式電加熱爐對牛乳樣品進行消化,在加入適量廉價的催化劑后,將消化爐的電壓調至220v 時,消化一份牛乳樣品僅需 100~105min。試驗結果表明,本方法具有精密(變異系數=0.62%)、準確、穩定、簡單、快速、安全等優點,可以滿足批量樣品的檢測需要,下面一起學習一下利用凱氏定氮儀測量牛乳中蛋白質的含量。
蛋白質是復雜的含氮有機化合物,主要是由各種氨基酸構成。它是牛乳的重要組成成分,亦是重要的營養物質。蛋白質的法定測定方法,以凱達爾氏發明的定氮法為基礎,根據各種蛋白質皆各有固定比數的氮這一事實,通過對氨的測定而推算出蛋白質含量,此法所得的含氮量除了確實屬于蛋白質組成成分的氮以外,還包括非蛋白質組成的其他有機及無機態氮,所以換算所得的蛋白質含量稱作為粗蛋白含量。蛋白質測定儀就是利用這一經典的測定蛋白質含量的方法研發制成,所得結果準確、穩定,但測定時間較長,一般一份樣品至少需要6~8h 始得結果。本文采用井式電加熱爐,增大消化管的受熱面積,使消化管內的試樣及濃H2SO4在井式電加熱爐內取得最大的熱效應,同時在消化前置入適宜的廉價催化劑,從而大大縮短了消化時間。
本文采用的方法能對牛乳中的蛋白質進行快速測定。牛乳中的蛋白質是含氮的有機化合物,樣品與硫酸和催化劑一同加熱消化,使蛋白質分解,分解的氨與硫酸結合生成硫酸銨,然后堿化蒸餾使氨游離,用硼酸吸收后再用鹽酸標準溶液滴定,根據酸的消耗量計算出氮的含量,再乘以換算系數即得蛋白質含量。
儀器設備與試劑:KDN—08A定氮儀(浙江托普儀器有限公司);電子分析天平;硫酸(H2SO4,分析純,比重1.84);硫酸銅(CuSO45H2O,分析純);硫酸鉀(K2SO4,分析純);40%氫氧化鈉(NaOH);2%硼酸(H3BO3);1mol/L 鹽酸(HCl);混合指示劑:0.1%甲基紅乙醇溶液+0.5%溴甲酚綠乙醇溶液(1∶ 1 )。
樣品處理:精確稱取樣品5.0g于消化管中,加入0.5gCuSO45H2O、5.0gK2SO4,再沿消化管壁徐徐加入10mlH2SO4(比重1.84),并輕輕搖蕩,使樣品全部被脫水炭化。
消化:將消化管分別放入消化架各個孔內,然后置于消化爐上,并立即開啟抽吸泵水閥,使抽吸泵處于吸氣狀態。接通電源,在加熱初始階段,須注意觀測,防止試樣因急沸而飛濺(初化時,電壓調至180~190v)。待泡沫停止后,將電壓調至220v,消化100~105min后冷卻。
蒸餾:
①在250ml 三角接受瓶中加入2%H3BO3 50ml 和2~3滴混合指示劑,將此瓶套在蒸餾器的接收管上,并且讓管口浸沒在H3BO3溶液中。
②在冷卻后的消化管中加入 50~80ml 蒸餾水,40~50ml 40%NaOH 溶液。
③扳動蒸餾托盤架把需要蒸餾的消化管固定在托盤架上,然后開啟蒸汽開關,向消化管內注入蒸汽,進行蒸餾。待接受瓶液面高于 150ml 刻度時,將接受瓶下移,使接受瓶離開液面。繼續蒸餾半分鐘,用蒸餾水洗瓶沖洗出氣口,然后取下接受瓶,待滴定之用。滴定用 0.1mol/LHCl 標準溶液滴定接受瓶內的溶液,滴定溶液由綠色變成淡紫色時為止。記下消耗 HCl 的毫升數。
結果計算:

測定結果:
在消化管中加入供試樣品 5.0g,然后按照上述分析步驟進行測定(一次可以消化 8 個樣品),結果如表所示:
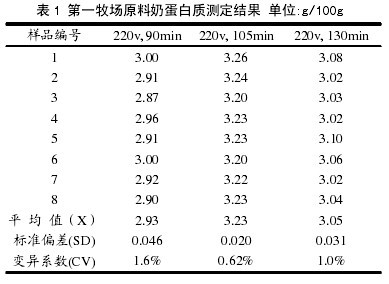
結論:
在用半微量凱氏定氮法測定牛乳中蛋白質的含量時,采用多孔井式電加熱爐,并在消化前置入適宜的廉價催化劑,對牛乳樣品進行消化,極大地提高了消化樣品的熱效應,同時將消化時間亦縮短了很多。牛乳蛋白質中含有7.1%(質量分數)的賴氨酸和2.6%(質量分數)的組氨酸,這兩種氨基酸中的氮在短時間內不易消化完全,往往導致總氮量偏低。消化時間過長會引起氨的損失。用本法測定牛乳中的蛋白質,消化一個樣品的時間為100~105min,變異系數為0.62%。本方法所得結果精密、準確、穩定、簡單、快速、安全,可以滿足批量樣品的檢測需要。




